Az Ataluren (PTC124™, 3-[5-(2-fluorophenyl)-1,2,4-oxadiazol-3-yl]benzoil sav) a genetikai mutáció következtében szintetizált működésképtelen fehérje képződés ellen kikísérletezett gyógyszer a leolvasás tekintetében nonszensz (értelmezhetetlen) pontmutáció esetén.
A nonszensz pontmutációra jellemző, hogy idő előtt leállítja a fehérjeszintézist:
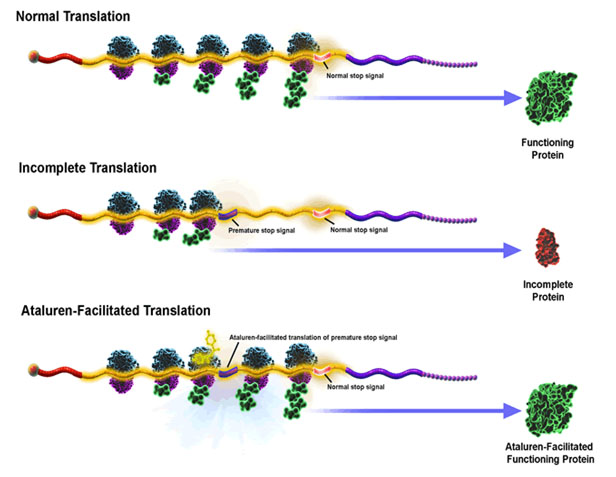
A genetikai mutáció okozta betegségek 5-15%-át nonszensz pontmutációk okozták. Ilyen a Duchenne szindróma is.
Az Ataluren kiiktatja a pontmutáció okozta idő előtti stop kódot, (a hatékonyság sorrendjében: UGA, ezt követi az UAG és az UAA ) és ennek eredményeképp a transzláció tovább folytatódik egészen a normál, valódi stop kódig. Végül funkcionáló fehérje keletkezik. Eközben a mRNS stabilitása és az átírás sem változik.
Az ataluren szájon át bevehető, kis molekulájú, nem toxikus, nem módosítja a beteg genetikai kódját, és nem módosítja a normál stop jelet.
Forrás: http://www.ptcbio.com
A pontmutációs DMD betegeknél az ataluren klinikai kipróbálása már folyamatban van az USÁ-ban. A koncepció helyességét a klinikai kipróbálás 2a fázisa igazolta. 38 fiú 28 napig kapott ataluren kezelést. Vizsgálatok: izombiopszia, keratin kináz aktivitás mérése. A betegek 47%-ában kimutatható volt a disztrofin koncentráció növekedése a pontmutáció helyétől függetlenül. A betegek keratin kináz aktivitása csökkent, az izmok sérülékenysége csökkent, aktivitásuk nőtt.
Forrás: http://www.bio-medicine.org/medicine-technology/PTC-Therapeutics-Announces-Additional-Positive-Interim-Phase-2-0AResults-of-PTC124-in-Duchenne-Muscular-Dystrophy-780-3/
2008 febr- 2010 aug és 2009 jan-2011 dec között zajlik két klinikai 2b kipróbálás. Az első eredmények 2010 áprilisában várhatók. A két kipróbálás részvevői minimum 5 éves, legalább 75 méter megtételére képes 165 illetve 174 fiúgyerek. Az egyik kísérletben PTC124 magas dózist, alacsony dózis hatását próbáltak ki, illetve a második kísérletben napi 3x20 mg/kg dózist kapnak a paciensek. Gyógyszeradagolás napi három alkalommal történik, étkezés után, az egyik alkalommal 48 illetve a másik alkalommal 96 héten keresztül. Ez alatt az idő alatt a betegek folyamatos klinikai ellenőrzés alatt állnak.
Forrás: http://clinicaltrials.gov
A vizsgálatot szervező cég a PTC Therapeutics, Inc. (PTC). A Muscular Dystrophy Association (MDA) — $1.5 millió dollárral támogatja a gyógyszerfejlesztést.
http://www.ptcbio.com

